Hoe Bereken Je De Reactiewarmte Bij Scheikunde?
Table of Contents
De Reactiewarmte Berekenen Met De Vormingswarmte – Scheikundelessen.Nl
Keywords searched by users: hoe bereken je de reactiewarmte scheikunde reactiewarmte berekenen met vormingswarmte, hoe bereken je de vormingswarmte, reactiewarmte berekenen binas, reactie-energie formule, reactiewarmte oefenen, formule vormingswarmte scheikunde, reactiewarmte endotherm of exotherm, verschil reactiewarmte en vormingswarmte
Hoe bereken je de reactiewarmte in de scheikunde?
Reactiewarmte is een belangrijk concept in de scheikunde. Het verwijst naar de hoeveelheid energie die vrijkomt of geabsorbeerd wordt tijdens een chemische reactie. Het begrijpen en kunnen berekenen van reactiewarmte is van cruciaal belang voor het begrijpen en optimaliseren van chemische processen. In dit artikel zullen we bespreken hoe je de reactiewarmte kunt berekenen, inclusief het gebruik van vormingswarmte, en enkele veelgestelde vragen over dit onderwerp beantwoorden.
Wat is reactiewarmte?
Reactiewarmte, ook wel bekend als reactie-energie, is de hoeveelheid energie die vrijkomt of geabsorbeerd wordt tijdens een chemische reactie. Het kan worden beschouwd als de energieverandering die optreedt wanneer de reactanten worden omgezet in producten. Reactiewarmte kan zowel positief als negatief zijn, afhankelijk van het feit of er energie wordt geabsorbeerd (endotherme reactie) of vrijkomt (exotherme reactie) tijdens de reactie.
De eenheden van reactiewarmte
Reactiewarmte wordt meestal uitgedrukt in joules (J) per mol van de reactie. De hoeveelheid energie die vrijkomt of geabsorbeerd wordt, hangt af van de hoeveelheid stof die bij de reactie betrokken is, vandaar dat het vaak wordt uitgedrukt in eenheden van energie per mol.
Hoe bereken je de reactiewarmte?
Er zijn verschillende manieren om de reactiewarmte te berekenen, afhankelijk van de beschikbare informatie. Een veelgebruikte methode is het gebruik van Hess’s wet, die stelt dat de totale verandering in enthalpie van een reactie gelijk is aan de som van de veranderingen in enthalpie van de afzonderlijke stappen van de reactie.
Om Hess’s wet toe te passen, moeten de enthalpieën van de betrokken stoffen bekend zijn. Deze kunnen worden gevonden in referentietabellen of worden berekend met behulp van experimentele gegevens. Door de veranderingen in enthalpie van de bekende reacties te combineren, kan de totale verandering in enthalpie, en dus de reactiewarmte, worden berekend.
Een andere methode om reactiewarmte te berekenen is door de enthalpieën van de reactanten af te trekken van de enthalpieën van de producten. Dit geeft de verandering in enthalpie van de reactie, die overeenkomt met de reactiewarmte. Deze methode kan worden toegepast als de enthalpieën van zowel de reactanten als de producten bekend zijn.
Reactiewarmte berekenen met vormingswarmte
Een andere benadering om de reactiewarmte te berekenen is door gebruik te maken van vormingswarmte. Vormingswarmte is de enthalpieverandering die optreedt wanneer één mol van een zuivere stof wordt gevormd uit de elementen in hun meest stabiele vorm.
Om de reactiewarmte te berekenen met behulp van vormingswarmte, moet je de vormingsenthalpieën van de reactanten en de producten kennen. De reactiewarmte kan dan worden berekend door de vormingsenthalpieën van de reactanten af te trekken van de vormingsenthalpieën van de producten, en de reactiewarmte per mol te verkrijgen.
Reactiewarmte berekenen met behulp van Binas
Binas is een naslagwerk dat vaak gebruikt wordt bij het berekenen van reactiewarmte. Binas bevat tabellen met informatie over de fysische en chemische eigenschappen van verschillende stoffen, waaronder enthalpieën. Door de juiste informatie op te zoeken in Binas, kun je de enthalpieën van de betrokken stoffen vinden en de reactiewarmte berekenen.
Reactiewarmte bij endotherme en exotherme reacties
Bij een exotherme reactie komt er energie vrij in de vorm van warmte. Dit betekent dat de reactiewarmte negatief is, omdat de energie wordt “afgegeven” aan de omgeving. Bij een endotherme reactie wordt er juist energie geabsorbeerd uit de omgeving, waardoor de reactiewarmte positief is.
Het verschil tussen endotherme en exotherme reacties kan worden weergegeven in een energiediagram. Bij een exotherme reactie bevindt de reactie-energie zich op een lager energieniveau dan de energie van de reactanten, terwijl bij een endotherme reactie de reactie-energie hoger is dan de energie van de reactanten.
Toepassingen van reactiewarmte
Reactiewarmte heeft verschillende toepassingen in de chemie en industrie. Een van de belangrijkste toepassingen is bij het ontwerpen van chemische reactoren. Door de reactiewarmte te berekenen, kunnen ingenieurs de juiste omstandigheden creëren om reacties efficiënt te laten verlopen.
Daarnaast wordt reactiewarmte gebruikt bij het optimaliseren van reactieomstandigheden. Door de reactiewarmte te begrijpen, kunnen chemische processen worden aangepast om de gewenste resultaten te bereiken.
Bovendien is reactiewarmte belangrijk bij het begrijpen van energieveranderingen tijdens chemische processen. Het kan informatie bieden over de efficiëntie van een reactie en kan worden gebruikt om de theoretische maximale opbrengst van een reactie te berekenen.
Veelvoorkomende valkuilen bij het berekenen van reactiewarmte
Bij het berekenen van reactiewarmte zijn er enkele veelvoorkomende valkuilen waar je op moet letten. Ten eerste is het belangrijk om de juiste enthalpieën van de betrokken stoffen te gebruiken. Deze kunnen variëren afhankelijk van de temperatuur en druk, dus zorg ervoor dat je de juiste waarden gebruikt.
Daarnaast moet je rekening houden met eventuele faseveranderingen die optreden tijdens de reactie. Faseveranderingen, zoals het verdampen van een vloeistof of het condenseren van een gas, vereisen extra energie en kunnen de reactiewarmte beïnvloeden. Zorg ervoor dat je deze factoren in overweging neemt bij het berekenen van de reactiewarmte.
Tot slot is het belangrijk om de juiste eenheden te gebruiken en om eenheden correct om te rekenen. Zorg ervoor dat je de eenheden van de enthalpieën van de stoffen en de reactiewarmte op elkaar afstemt, zodat je nauwkeurige berekeningen kunt maken.
FAQs
Wat is het verschil tussen reactiewarmte en vormingswarmte?
Reactiewarmte verwijst naar de totale energieverandering die optreedt tijdens een chemische reactie, terwijl vormingswarmte de enthalpieverandering is die optreedt wanneer één mol van een zuivere stof wordt gevormd uit de elementen in hun meest stabiele vorm. Reactiewarmte kan worden berekend door de enthalpieën van de reactanten af te trekken van de enthalpieën van de producten, terwijl vormingswarmte wordt berekend door de vormingsenthalpieën van de reactanten af te trekken van de vormingsenthalpieën van de producten.
Hoe kan ik oefenen met het berekenen van reactiewarmte?
Een goede manier om te oefenen met het berekenen van reactiewarmte is door gebruik te maken van oefenopgaven. Deze opgaven geven je de kans om de verschillende methoden en formules toe te passen die nodig zijn om reactiewarmte te berekenen. Je kunt oefenopgaven vinden in scheikundeboeken, online oefenplatforms of oefenexamens.
Wat is de formule voor reactie-energie?
De formule voor reactie-energie is Q = delta H, waarbij Q de reactiewarmte is en delta H de verandering in enthalpie van de reactie.
Wat is de formule voor vormingswarmte in de scheikunde?
De formule voor vormingswarmte in de scheikunde is delta H = Hproducten – Hreactanten. Hierbij is delta H de verandering in enthalpie, Hproducten de enthalpie van de producten en Hreactanten de enthalpie van de reactanten.
Is reactiewarmte altijd endotherm of exotherm?
Reactiewarmte kan zowel endotherm als exotherm zijn, afhankelijk van de reactie. Bij een exotherme reactie komt er energie vrij in de vorm van warmte, wat resulteert in een negatieve reactiewarmte. Bij een endotherme reactie wordt er energie geabsorbeerd uit de omgeving, wat resulteert in een positieve reactiewarmte.
Wat is het verschil tussen reactiewarmte en vormingswarmte?
Reactiewarmte verwijst naar de totale energieverandering die optreedt tijdens een chemische reactie, terwijl vormingswarmte de enthalpieverandering is die optreedt wanneer één
Categories: Gevonden 10 Hoe Bereken Je De Reactiewarmte Scheikunde
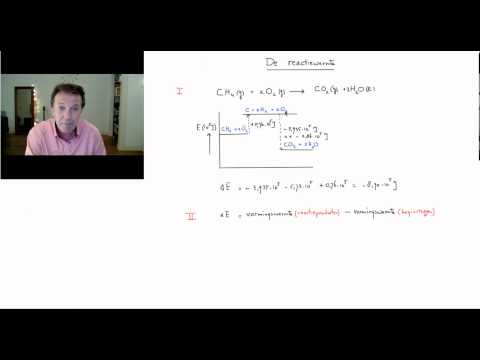
De reactie-energie Q kan berekend worden met deze formule: Q = c · m · ΔT. Bijvoorbeeld: los 10 gram natriumhydroxide op in 100 mL water.Reactiewarmte = delta E, de hoeveelheid energie die vrijkomt of de hoeveelheid energie die nodig is bij een chemische reactie. De eenheid is J/mol.Het verschil tussen het beginniveau van energie en het eindniveau van energie noem je het energie-effect. Het beginniveau van energie (E1), het eindniveau van energie (E2) en het energie-effect (delta E) worden weergegeven in een energiediagram.
- Schrijf de reactievergelijking op.
- De stoffen voor de reactiepijl moeten worden ontleed, zoek dit op in je BiNaS. …
- Zoek de vormingswarmten op van de reactieproducten.
- Reken ΔE uit door alles bij elkaar op te tellen.
Hoe Weet Je De Vormingswarmte?
Om de vormingswarmte te achterhalen, moet je een aantal stappen volgen.
Ten eerste, schrijf de reactievergelijking op. Zorg ervoor dat de stoffen op de reactiepijl worden ontleed. Hiervoor kun je de informatie in je BiNaS raadplegen.
Ten tweede, zoek de vormingswarmten op van de reactieproducten. Dit kan ook worden gevonden in je BiNaS.
Tot slot, reken de verandering in energie (ΔE) uit door de vormingswarmten van de reactieproducten bij elkaar op te tellen.
Wat Is Delta E Scheikunde?
In de scheikunde verwijst Delta E naar het verschil tussen het beginniveau van energie (E1) en het eindniveau van energie (E2). Dit verschil, ook wel het energie-effect genoemd, kan worden weergegeven in een energiediagram. Het energiediagram geeft visueel weer hoe de energie verandert tijdens een chemische reactie. Door het bestuderen van Delta E kunnen scheikundigen inzicht krijgen in de energieovergangen die plaatsvinden bij verschillende chemische processen.
Wat Is De Vormingswarmte Van Glucose?
Details 30 hoe bereken je de reactiewarmte scheikunde






See more here: brokengroundgame.com
Learn more about the topic hoe bereken je de reactiewarmte scheikunde.
- Reactiewarmte – Wikipedia
- Samenvatting SK H4 – Zuur-base, PH, reactiewarmte (exotherm en …
- Reactie energie – Mr. Chadd Academy
- Endotherme en exotherme processen – Bijles Scheikunde HAVO
- Examen VWO
- Reactiewarmte – Wikipedia
See more: https://brokengroundgame.com/music/

